cód. #7439
FUVEST - Química - 2018 - Vestibular - Primeira Fase
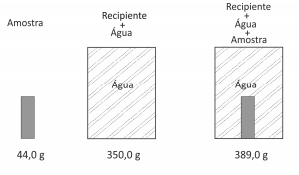
Um antiácido comercial em pastilhas possui, em sua composição, entre outras substâncias, bicarbonato de sódio, carbonato de sódio e ácido cítrico. Ao ser colocada em água, a pastilha dissolve‐se completamente e libera gás carbônico, o que causa a efervescência. Para entender a influência de alguns fatores sobre a velocidade de dissolução da pastilha, adicionou‐ se uma pastilha a cada um dos quatro recipientes descritos na tabela, medindo‐se o tempo até a sua dissolução completa.
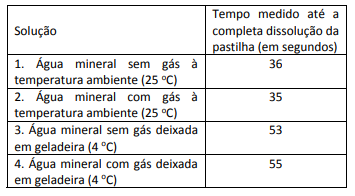
Para todos os experimentos, foi usada água mineral da mesma marca. Considere a água com gás como tendo gás carbônico dissolvido.
Com base nessas informações, é correto afirmar que
A) o uso da água com gás, ao invés da sem gás, diminuiu a velocidade de dissolução da pastilha em cerca de 50%, uma vez que, como já possui gás carbônico, há o deslocamento do equilíbrio para a formação dos reagentes.
B) o uso da água com gás, ao invés da sem gás, aumentou a velocidade de dissolução da pastilha em cerca de 33%, uma vez que o gás carbônico acidifica a água, aumentando a velocidade de consumo do carbonato de sódio.
C) nem a mudança de temperatura nem a adição de gás carbônico na solução afetaram a velocidade da reação, uma vez que o sistema não se encontra em equilíbrio.
D) o aumento da temperatura da água, de 4 °C para 25 °C, levou a um aumento na velocidade da reação, uma vez que aumentou a frequência e a energia de colisão entre as moléculas envolvidas na reação.
E) o aumento da temperatura da água, de 4 °C para 25 °C, levou a um aumento na velocidade da reação, uma vez que facilita a liberação de gás carbônico da solução, deslocando o equilíbrio para a formação dos reagentes.
A
B
C
D
E