cód. #11105
IF-MT - Química - 2018 - Vestibular
Basicamente, o vidro é obtido a partir de uma reação de fusão a 1500 °C entre o carbonato de sódio (Na2CO3), conhecido como barrilha, o calcário (CaCO3) e a sílica presente na areia (SiO2):
Na2CO3 + CaCO3 + SiO2 → silicatos de sódio e cálcio (vidro comum) + gás carbônico.

(Fonte: http://alunosonline.uol.com.br/quimica/curiosidades-sobre-vidro.html Acesso em jan. 2018.)
Ele é um tipo de material dos mais utilizados nas tarefas do dia a dia, não é biodegradável e pode ser reciclado várias vezes sem, no entanto, perder suas características e propriedades.
Com base nas informações do texto e com o propósito de atenuar os danos ambientais causados pelo descarte de materiais de vidro, tem-se que
A) quando reciclamos o vidro ou compramos vidro reciclado, estamos contribuindo com o meio ambiente, pois este material deixa de ir para os aterros sanitários ou para a natureza (rios, lagos, solo, matas).
B) a reciclagem de vidro não é capaz de gerar renda para as pessoas que atuam em cooperativas de catadores e recicladores de vidro e de outros materiais reciclados, considerando que os plásticos é que apresentam rentabilidade financeira ao serem coletados
C) para garantir as características e qualidades do vidro reciclado, assim como as de outros tipos de materiais, não se considera importante a separação e coleta seletiva, uma vez que, ao ser aquecido, qualquer tipo de material sofrerá decomposição térmica.
D) a principal matéria-prima usada na produção de todos os tipos de vidro é o SiO2 (trióxido de silício).
E) por não ser biodegradável, o homem deveria substituir o uso do vidro pelo uso dos plásticos, pois esses, na sua grande maioria, são biodegradáveis.
A
B
C
D
E


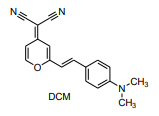 A respeito da estrutura do DCM são feitas três afirmativas: I. Apresenta dois carbonos com geometria linear II. Conta em sua estrutura com as funções orgânicas amida e éter. III. Existem apenas seis hidrogênios.
A respeito da estrutura do DCM são feitas três afirmativas: I. Apresenta dois carbonos com geometria linear II. Conta em sua estrutura com as funções orgânicas amida e éter. III. Existem apenas seis hidrogênios. 